Bolsista: Litton Jr.
Em química, matéria significa qualquer coisa que possui massa, ocupa lugar no espaço físico e está sujeito a inércia. A matéria é aquilo que existe, e é sempre constituída de partículas elementares com massa não-nula.
As propriedades da matéria são observadas em qualquer corpo, independente da substância de que é feita.
Fases ou estados da matéria
A matéria é composta por pequenas partículas e, de acordo com o maior ou menor grau de agregação entre elas, pode ser encontrada em três estados: sólido, líquido e gasoso. O volume, a densidade e a forma de um composto podem variar com a temperatura, sendo assim, os compostos apresentam características de acordo com o estado físico em que se encontram, veja as características de cada um:
- Estado Sólido: as moléculas da matéria se encontram muito próximas, sendo assim possuem forma fixa, volume fixo e não sofrem compressão. Por exemplo: em um cubo de gelo as moléculas estão muito próximas e não se deslocam.
- Estado Líquido: as moléculas estão mais afastadas do que no estado sólido e os elementos que se encontram nesse estado possuem forma variada, mas volume constante. Além dessas características, possui facilidade de escoamento e adquirem a forma do recipiente que os contém.
- Estado Gasoso: a movimentação das moléculas nesse estado é bem maior que no estado líquido ou sólido. Se variarmos a pressão exercida sobre um gás podemos aumentar ou diminuir o volume dele, sendo assim, pode-se dizer que sofre compressão e expansão facilmente. Os elementos gasosos tomam a forma do recipiente que os contém.
Essas características obedecem a fatores como a Força de Coesão (faz com que as moléculas se aproximem umas das outras) e a Força de Repulsão (as moléculas se afastem umas das outras). No estado gasoso a Força de Repulsão predomina, enquanto que no estado sólido é a Força de Coesão. Assim, quando uma substância muda de estado físico sofre alterações nas suas características microscópicas (arranjo das partículas) e macroscópicas (volume, forma), sendo que a composição continua a mesma.
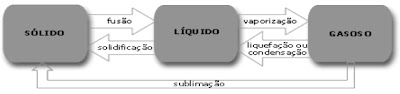
Mudanças de Estado Físico
Na natureza, as substâncias podem ser encontradas em três diferentes fases, as quais são denominadas de fase sólida, fase líquida e fase gasosa. Os fatores que determinam o estado em que as substâncias se encontram são a temperatura e a pressão. Ou seja, para cada fase os materiais possuem temperatura e pressão diferente. Por exemplo, o ferro em condições ambientes apresenta-se no estado sólido, mas se elevarmos a sua temperatura, passará a ser líquido. O mesmo acontece com a água. Em condições ambiente esta substância se encontra no estado líquido, contudo, se abaixarmos a sua temperatura, passará para o estado sólido.
Substância química
São átomos ligados entre si. Temos como exemplo o oxigênio, hidrogênio, etc. Quando é formada por um elemento, a substância é chamada de simples. E, quando formada por dois ou mais elementos é denominada de substância composta.
Fenômeno Físico e Químico
Fenômeno é toda e qualquer transformação que ocorre com a matéria, ocorrendo mudanças qualitativas na composição. Os fenômenos podem ser classificados como físico ou químico.
Fenômeno físico:
É toda transformação em que não há alteração na composição química, ou seja, não há formação de novas substâncias. Nele, as propriedades da matéria, como ponto de fusão e ebulição, não se alteram.
Exemplos:
- ao rasgar um papel ele continua sendo o mesmo papel, mesmo que sua forma mude.
- fusão do gelo
- dilatação dos corpos
Fenômeno químico:
Nesse tipo de fenômeno, ocorre a formação de novas substâncias, alterando a natureza da matéria, impedindo a recuperação da substância. São chamados também de reações químicas, representadas graficamente pelas equações químicas.
Aspectos observados diante de transformações ou reações químicas:
• A liberação de gases;
• Alteração na coloração;
• Mudança de energia térmica (reações exotérmicas e endotérmicas);
• Formação de precipitado.
Substância Pura e Mistura
Substância pura é aquela formada exclusivamente por partículas (moléculas ou átomos) quimicamente iguais.
As substâncias puras podem ser simples ou compostas.
Já a mistura é qualquer sistema formado por duas ou mais substâncias puras, denominadas componentes. Pode ser homogênea ou heterogênea. Toda mistura homogênea é uma solução. Ou ainda, a mistura á a junção de duas ou mais substâncias puras em, onde cada substância continua com as suas características iniciais.
Bom, essa é a matéria da semana, espero que possa ajudar vocês blogueiros do QUIPIBID! Até o próximo post.




Deveria ser explicado mais detalhadamente, mas se for apenas um texto para se ter uma noção superficial, está bom.
ResponderExcluirEu gostei!
ResponderExcluirVamos à realidade. O texto esta de excelente nível e na medida certa para criar no aluno o interesse, se houver, de buscar mais detalhes; porem, o suficiente para a realização dos exercicios e do que se cobra em vestibulares e enem.
ResponderExcluirEu achei bem interessante
ResponderExcluirBom mesmo