Bolsista:
Darlyane Ribeiro
Olá
caros leitores!
Água,
incolor, inodora, insípida, teria tudo para ser simplesmente mais uma
substância, mas pelo contrário, particularmente uma das mais importantes, de
todo planeta. Ela é encontrada nos três estados físicos, sólido, líquido e
gasoso. Nosso corpo é composto por 70% de água, que é responsável pelo
desempenho de uma boa digestão onde produz enzimas melhorando as reações
químicas, pela eliminação de dejetos, regulação e harmonização das funções
corpóreas.
Maior
parte do nosso planeta é composta por essa substância.
Com
essas características, como a água pode ser tão fundamental para a vida? Ela é
motivo de muitas pesquisas, ainda não se sabe tudo sobre ela.
É
importante como alimento, necessária para a higienização do nosso corpo, limpeza
de utensílios e diversas outras coisas. Já foi considerada pelos gregos
antigos, um dos elementos fundamentais da matéria, juntamente com, fogo, terra
e ar como podemos ver na figura 1, acreditava-se que esses elementos eram os
únicos, que esses formavam a matéria originando o físico. [1], [6] e [7]
Figura
1:
Quatros elementos fundamentais de Aristóteles.
Fonte: http://professorbiriba.com.br/boilerplate/html/primeiro_ano/fasciculo1/nivel-azul/pagina2-azul.html
Antes
era considerado um elemento, mais tarde descobriu-se que era uma substância
composta por dois tipos de átomos, o oxigênio e o hidrogênio. A sua estrutura
molecular é simples, suas ligações são covalentes, onde o hidrogênio compartilha
seu elétron com o oxigênio e o outro hidrogênio compartilha seu elétron com o oxigênio,
assim a molécula fica estabilizada, o oxigênio com oito elétrons e o hidrogênio
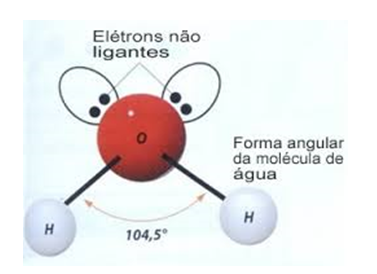
com dois elétrons. A forma da molécula é angular, como podemos ver na figura 2.
[2], [3], [4] e [5]
Na
figura 2, podemos observar que há um deslocamento nos átomos de hidrogênio,
isso se deve a nuvem eletrônica dos pares de elétrons não ligantes do oxigênio,
criando uma força de repulsão deslocando os hidrogênios. Esta molécula é polar,
ela possui uma desigualdade de densidade de elétrons. Nos pares de elétrons não
ligantes do oxigênio possui uma carga parcial negativa, e no hidrogênio possui
uma carga parcial positiva. [2]
Figura
2:
Ligação molecular da água.
Fonte:
http://www.alunosonline.com.br/quimica/agua-substancia-interessante.html
Esta
molécula também faz uma ligação de hidrogênio, que é quando o hidrogênio faz
uma ligação com elemento muito eletronegativo, que no caso é o flúor, oxigênio
e nitrogênio. Como na molécula da água existe ligação hidrogênio e oxigênio,
consequentemente ela é ligação de hidrogênio. Esta ligação faz com que a água
seja diferente de várias outras substâncias, como por exemplo, a flutuação do
gelo, elevado calor de vaporização, tensão superficial como podemos ver na
figura 3. Com relação a outras substâncias à mesma temperatura, ela é capaz de
ganhar ou perder maior quantidade de calor, além de ser um solvente universal,
pois ela dissolve quase todas as substâncias existentes na natureza. O que a
faz ser eficiente como solvente, é por ser uma molécula angular, tornando-a polarizável.
[1] e [2]
Figura
3:
tensão superficial da água.
Fonte:
http://www.brasilescola.com/quimica/tensao-superficial-agua.htm
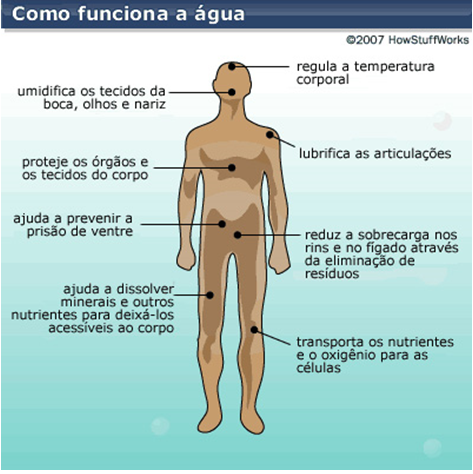
Quando
o calor aumenta, ou se tem febre, diarreia entre outros, há uma necessidade maior
de ingerir água, pois nesses casos a perda de água acontece em maior
quantidade. Por dia é recomendado de 30 a 35 ml de água por kg do peso
corpóreo, por dia. Nosso corpo não possui a capacidade de armazenar água, ou
seja, a cada dia devemos repor. A água é tão importante para nosso organismo,
que ele sem água funciona por apenas dois ou três dias, a falta da água em
nosso corpo, causa maior dano que por falta de qualquer outro nutriente. A ação
da água em nosso corpo pode ser vista na figura 4. [6], [7] [8]
Figura 4: Ação
da água no corpo humano.
Fonte: http://www.blogdoperetz.com.br/dica-da-semana-cuidados-com-a-hidratacao/
Lembrando
que a água que ingerimos não é apenas H2O, existem outros
componentes nela, como minérios. Apenas H2O é praticamente impossível
de encontrar na natureza. Seu ponto de ebulição é a 100°C e seu ponto de fusão
é a 0°C e seu ponto de solidificação é a 0°C.
Bibliografia:
[1] FOGAÇA Jennifer Rocha Vargas. Teoria dos Quatro Elementos. Disponível em: http://www.soq.com.br/conteudos/ef/agua/p3.php
acessado dia 29/09/2015 às 17:00.
[2]
LOPES, Cesar Valmor Machado. NETO, Odone Gino Zago. Águas. Universidade Federal do Rio
Grande do Sul . Instituto de química. Disponível em: http://www.iq.ufrgs.br/aeq/html/publicacoes/matdid/livros/pdf/aguas.pdf
acessado dia 28/09/2015 às 15:10
[3] SANTOS,Vanessa
Sardinha dos. Composição química
da água. Disponível em: http://www.mundoeducacao.com/biologia/composicao-agua.htm Acessado dia 28/09/2015 às 15:15
[4] STEFANELLI, Armandina
J. M. Molécula da água. Disponível
em: http://www.stefanelli.eng.br/webpage/p-molecula-agua.html
acessado dia 28/09/2015 às 15:13
[5] GOMES, Abílio
Soares. CLAVICO, Etiene. Propriedades
Físico-Químicas da Água. Departamento de biologia marinha. 2005. Disponível
em: http://www.uff.br/ecosed/PropriedadesH2O.pdf
acessado dia
28/09/2015 às 15:00.
[6]SERAFIM, Ana
Lúcia; VIEIRA, Eilamaria, Libardoni; LINDEMANN, Ivana Lorain; A importância da água no organismo humano.
2004. P. 147-157. Disponível em: http://sites.unifra.br/Portals/35/Artigos/2004/41/importancia.pdf
Acessado dia
09/10/2015
às 09:00
[7]BERTONI, Camila B de Souza; BERTONI, Luiz Carlos. Água: a importância da hidratação.
Clínica de tratamento de dor crônica, problemas emocionais. Paraná. Disponível
em: http://www.bodytalklondrina.com.br/docs/179.pdf acessado dia 09/10/2015 às 09:15
[8] A
importância da água para o organismo humano. 2014. Disponível
em: http://www.bensaude.com.br/noticias/leitura/433/A-import%C3%A2ncia-da-%C3%A1gua-para-o-organismo-humano
acessado dia 09/10/2015 Ás 11:40



Nenhum comentário:
Postar um comentário